BSCDC
百色市从2023年起,已经顺利开展疫苗临床试验工作。目前,有百色市疾病预防控制中心、靖西市疾病预防控制中心和隆林各族自治县疾病预防控制中心三个试验现场实施机构。
很多宝儿们可能会问:啥是临床试验?疾控中心能做临床试验?临床试验就是“小白鼠”试验吗?


图片来源:图怪兽设计
疾控中心能做疫苗临床试验吗?
《中华人民共和国疫苗管理法》(2019年国家主席令第30号)第十六条:国家鼓励符合条件的医疗机构、疾病预防控制机构等依法开展疫苗临床试验。
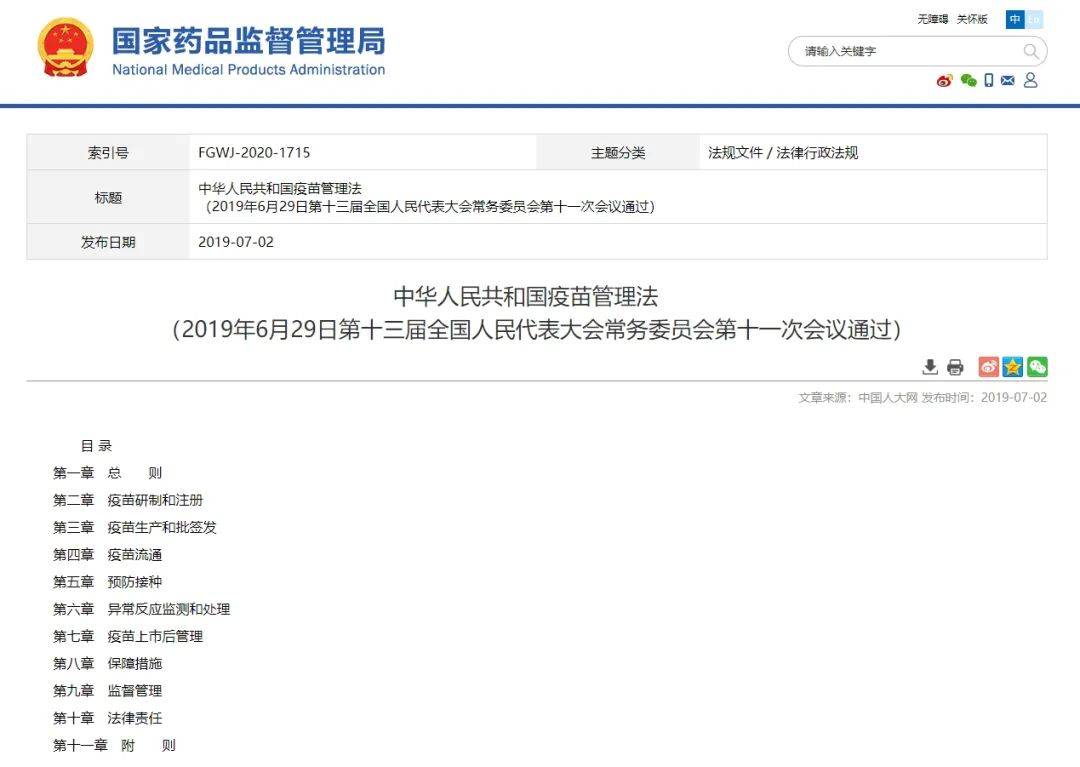
图片来源:国家药品监督管理局官网
△ 图为百色市疾控中心试验现场备案证明

临床试验就是“小白鼠”试验吗?

图片来源:国家药品监督管理局官网
临床前研究:毒株、细胞筛选是保证疫苗安全、有效、持续供应的基础保障。以病毒疫苗为例,实验室阶段需进行毒株的筛选、必要的毒株减毒、毒株对培育细胞基质适应及传代过程中的稳定性研究,并探索工艺质量稳定性,建立动物模型等。根据每个疫苗情况选择小鼠、豚鼠、兔或猴等进行动物试验。在初步提示工艺可控、质量稳定及安全有效的前提下,可以向国家药品监督管理部门申请进行临床试验。临床前研究一般需要5-10年。
(这个才是真正的“小白鼠”试验哦)
所以,新研发的疫苗,会先进行“小白鼠”试验,提示疫苗安全有效了,才能向国家药品监督管理部门申请进行临床试验的。
什么是疫苗临床试验?
申报临床:申请预防用疫苗临床试验,需向国家药品监督管理部门报送药学、药理毒理、临床等不同专业的研究资料。根据不同疫苗的情况,有时研究资料达200多本,其中包括疫苗毒株/细胞种子库建立、生产工艺研究、质量研究、稳定性研究、动物安全性评价和有效性评价以及临床试验方案等。生物制品药学、药理毒理学、临床等相关领域专家根据国家《药品注册管理办法》及疫苗相关的技术评价要求对全套研究资料进行技术审评,符合要求的获发疫苗临床试验批件。质量控制及安全有效性达不到临床试验要求的,需完善并补充各种试验或申报资料。有的申请会经过很多次的沟通补充完善,对涉及重大公共卫生的还要召开专家咨询会,直至申报资料符合要求,才会获发疫苗临床试验批件。
(所以,能获批进行临床试验的疫苗,疫苗的相关技术评价肯定是达标的哦)
注册临床试验:一般分为I/Ⅱ/Ⅲ期三个研究阶段。国家对疫苗人体临床试验有严格的管理规定,包括《药物临床试验质量管理规范》《疫苗临床试验质量管理指导原则》《伦理委员会药物临床试验伦理审查工作指导原则》《药品不良反应报告和监测管理办法》《疫苗临床试验技术指导原则》《临床试验数据管理工作技术指南》等等。各期临床试验从人员到现场以及监查都有严格的标准操作程序(SOP)要求。
I期临床试验:初步考察人体安全性,一般受试者为几十至百例。鉴于首次进行人体I期临床的重要性,国家专门发布《药物Ⅰ期临床试验管理指导原则》。若疫苗I期临床结果显示安全性良好,方可进行Ⅱ期临床试验。
Ⅱ期临床试验:主要进行疫苗的剂量探索研究,以及初步的有效性评价并考察进一步扩大人群后的安全性。一般受试者为几百到上千例。Ⅱ期临床试验达到预期目的后,方可进行Ⅲ期临床试验。
Ⅲ期临床试验:采用随机、盲法、安慰剂对照(或对照苗)设计,全面评价疫苗的有效性和安全性,一般受试者为数千到几万例不等。该期是疫苗上市获得注册批准的基础。若关键性Ⅲ期临床试验获得预期临床保护效果,安全性良好,企业方可将临床数据资料递交国家药品监督管理部门申报生产。
Ⅳ期临床试验:是疫苗注册上市后,对疫苗实际应用人群的安全性和有效性进行综合评价。是监测疫苗在大量目标人群常规使用状态下的各种情况,目的是发现不良反应并监控有效性/效力。
(所以,临床试验在疫苗上市前、上市后都会有开展的哦,都会一直对疫苗的安全性和有效性进行评价。)
百色市疫苗临床试验开展情况
目前,百色市疾控中心、靖西市疾控中心、隆林各族自治县疾控中心都有在开展不同疫苗的临床试验(主要为Ⅱ期、Ⅲ期和Ⅳ期),宝儿们可以多多关注哦~
-End-
「有用就扩散」
往期推荐
五价重配轮状病毒减毒活疫苗(Vero细胞)Ⅱ期临床研究招募开始了!
透支的肾,是补不回来的!这5个伤肾行为,很多人都在做!
快收藏,广西最新最全的预防接种单位信息来了!
手足口病高发季来临,我们应如何预防
▌来源:国家药品监督管理局
▌编辑:健康教育促进科
▌声明:科普内容及图片均来自网络及 各大主流媒体。版权归原作者所有,且仅用于科普公益宣传,如认为内容侵权,请联系我们删除,谢谢。